【AsianScientist】新しいバイオプロセス技術で細胞株開発を効率化
新しいバイオプロセス技術は、堅牢で収量の高い細胞株の開発を可能にし、生物医学研究と製薬イノベーションの進歩を支える。

どの段階であっても、発生する可能性のある障害を早期に認識することが、十分な情報に基づく意思決定と効率性改善の鍵となる。これは、科学的発見とイノベーションの中心となっている細胞株の開発に特に当てはまる。
生物医学的介入を臨床現場で実施する前に細胞株を使用すれば、がんなどのさまざまな疾病に薬剤候補の有効性を試験できる。細胞株は生きた環境であるため、複雑な代謝機構を利用することにより、バイオ医薬品製造の生成センターとしても機能する。例えば、科学者は細胞を誘導して、治療特性を持つ組換えたんぱく質などの望ましい生体分子を生成させることができる。
安定した生産的な細胞培養は、明らかにバイオ医薬品の製造プロセスに不可欠である。しかし、細胞株の開発には時間がかかり、技術的にも難しく、通常は12カ月から18カ月を必要とする。したがって、バイオテクノロジーの開発者は、潜在的な落とし穴を意識して、クローンのスクリーニングから細胞培養の拡大まで、可能な限り最善の決定を下すことができる先制的措置を講じる必要がある。これらの課題に対処するために、科学者とイノベーターは、開発のすべての段階で堅牢、高収量、かつ費用対効果の高い細胞株の開発を可能にする新しい技術を模索している。
のるかそるかの決断
科学者は細胞株開発の最初の段階から、すでに重要な決定を行わなければならない。細胞株の選択は、工程全体を左右する可能性がある。細胞は、特定の特徴と臨床機能を備えた生体分子を、持続的で生産性の高い方法で合成する必要がある。細胞がクローン集団に増殖したならば、高収量のクローンを選択するには、必然的に広範なスクリーニングと最適化が必要になる。
クローンの性能は予測不可能なため、開発者は時間をかけて膨大な数のクローンをスクリーニングし、安定性などのさまざまな指標を調べるために何度も検査を行う。さもないと、細胞培養増殖の収量が最適ではなくなり、あるいは生物学的産物の必要な特性を得られないなどが起こり、資源を浪費するかもしれない。
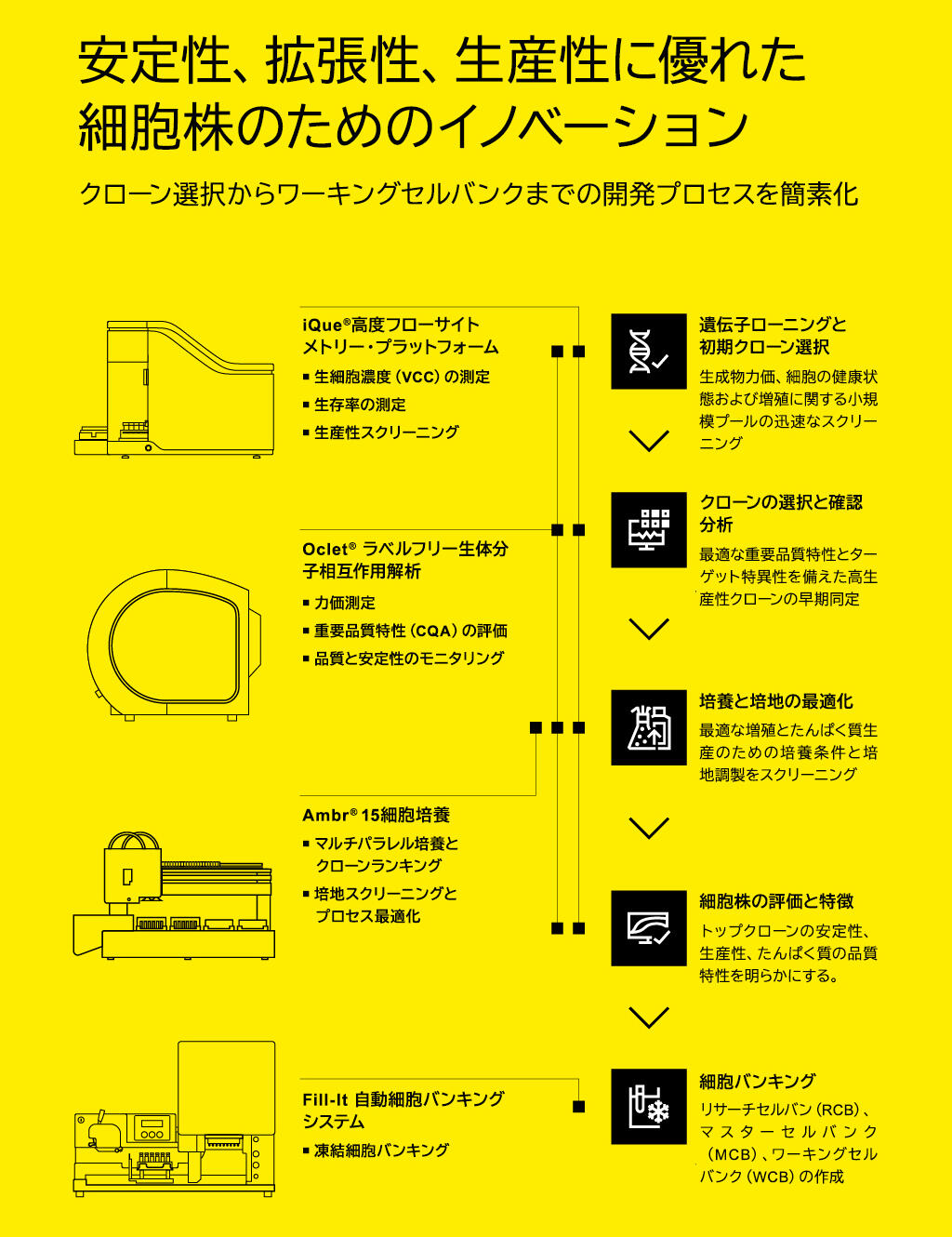
アジア等に展開するザルトリウス社(本部・ドイツ)が提供するiQue©は、高度ハイスループット・フローサイトメトリー・プラットフォームである。スクリーニングを加速し、科学者が最高性能を発揮する可能性の高いクローンを決定するのに役立つ。このプラットフォームは生細胞濃度を計算し、各クローンの分子的特徴を包括的に描き出す。このような分析は、最も生産性の高いクローンとそれに必要な培養条件を特定する鍵となる。また、ワンストップシステムであり、付属のiQue Forecyt© ソフトウェアを使えば、インタラクティブなゲーティングが可能であり、リアルタイムの結果を得ることができる。
効果的なクローン選択は、たんぱく質親和性や物理化学的特性などといった重要な品質属性の検査にも依存する。Octet® バイオレイヤー干渉法システムなどの機器はこの段階の鍵となり、最適なクローンの選択を指示するリアルタイムのラベルフリー分析を可能にする。その後、開発者は、細胞から合成された生物製剤の特徴を明らかにする必要性も出てくるかもしれない。そのために、ザルトリウス社の Octet© BLI 技術は、高速液体クロマトグラフィーや ELISA など他の技術よりも最大20倍速く力価親和性と濃度を測定できるようにしている。
細胞株技術でこれらのイノベーションを使うと、分析が迅速化され、スクリーニングで必要な最適化の回数を減らすことができる。そのため、開発者は細胞データを容易に分析し、最も望ましいクローンを選択し、プロジェクトを次の段階に進めることができる。
一貫した培養と特性評価
細胞培養を成功させるにあたり、環境条件と利用可能な栄養は、細胞の増殖速度と目的の生体分子を生成する能力に影響を与え、重要な役割を果たす。開発者はザルトリウス社の Ambr© プラットフォームなどのバイオリアクター技術を利用すれば、最適な培地条件を提供できる。これは統合システムを使えば科学者は複数の実験を管理し、複数のコロニーを同時に培養できるため、ワークフロー全体の効率が向上する。バイオリアクターは制御された環境としても機能し、性能を安定させ、高収量を可能にする。
この段階では、培養クローンとそれらが合成する分子生成物を評価するために、品質管理メカニズムと徹底的な監視戦略が重要になる。たとえば、製品は生体適合性がなければならない。つまり、人体に安全に導入できなければならない。特に製品が特定の臨床機能のために修飾されている場合、標準化を確保するために参照分子との比較が必要となることもある。
機能試験と安全性試験という異なる組み合わせ実施する場合は、通常、複数の機器と方法を使用する必要があり、小規模なバイオテクノロジー企業にとっては資源に負担がかかるであろう。この問題があるため、効率性が高く、包括的な特性評価が可能な統合分析技術の必要性が高まっている。さらに、将来の研究と製造を支えるために、特に規制基準を確実に守るためには、細胞株の特徴を定義し文書化することが不可欠である。
一貫性が鍵である
細胞株には、新しい、けれど先祖のクローンの属性を保つことのできる細胞を生産し続ける能力があるため、バイオ医薬品業界では非常に重要な存在となっている。細胞株の増殖中にこのような完全性を維持するために、保存の手順と施設は規制ガイドラインに準拠することが望ましい。現在、細胞株の保存には、細胞を凍結して生物学的特性を維持することが可能なクライオチューブ細胞バンキングが標準となっている。ただし、手動バンキング中の汚染リスクや、ラボ規模の製造と商業規模の製造との条件が異なることなど、いくつかの問題は残っている。
細胞株開発者は、手作業による処理よりも、迅速かつ一貫して高品質な細胞保存を促進できるザルトリウスのFill-Itシステムのような自動化プラットフォームの価値を認識している。自動化された細胞保存技術は、大量のバッチ間で条件を一定に保つことができ、細胞株開発および下流の生物学的製剤生産の拡張性を向上させるのに役立つ。
専用処理プラットフォーム
細胞株の供給をスケーラブルかつ持続可能なものにすることは、バイオ医薬品分野での科学的取り組みを継続的に支援するための鍵となる。しかし、生物製剤の製造は複雑であり、細胞株の開発プロセスも例外ではない。科学者やプロセスエンジニアは、厳しいスケジュール、絶え間ないコスト削減のプレッシャー、臨床までの時間の長さといった問題に直面している。
しかし、細胞株開発におけるイノベーションは、細胞特性に関する高品質のデータを提供し、多くの情報に基づいた意思決定を支援することで、これらの問題に対処できる。専用統合技術セットを使えば、開発の各段階で堅牢性を維持しつつ、開発者が効率を最大化することができる。最終的には、信頼性が高くスケーラブルな細胞株開発が、最先端の科学への道を開き、研究を商業的に実現可能であり臨床に影響を与える製品に変換することができる。
(2022年11月10日公開)






