【AsianScientist】 腫瘍の詳細なマッピング—胃がん個別化治療への一歩
この発見は、生存率を向上させ副作用を軽減する標的がん治療につながるかもしれない。(2025年7月16日公開)
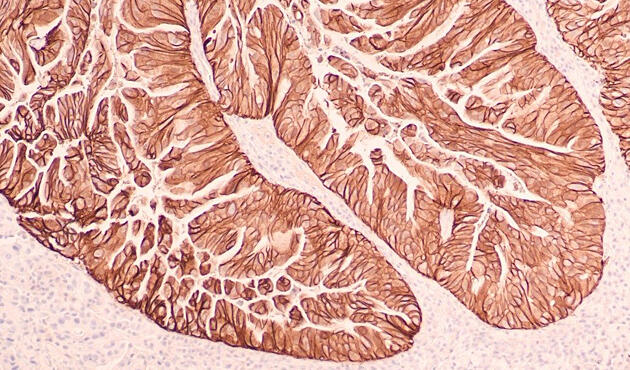
胃がんは世界的に見られる健康上の懸念となっている。世界で5番目に多いがんの種類であり、がん関連死因の第3位であり、毎年約77万人が亡くなっている。シンガポールだけでも、胃がんはがん関連死因の上位10位に入っており、年間約300人が亡くなっている。
しかし、シンガポールの科学者たちは、この病気に立ち向かう上で重要な発見をした。
シンガポール胃がんコンソーシアム(Singapore Gastric Cancer Consortium)の研究チームは、高度なマッピング技術を用いて胃腫瘍の詳細な「アトラス」を作成し、がん細胞の挙動、進化、そして環境との相互作用に関する隠れたパターンを明らかにした。
Cancer Discovery誌に発表されたこの研究は、患者の腫瘍の独特な構成に合わせて治療法を個別化することで、胃がんの診断法と治療法を変える可能性を秘めている。この研究内容は、正確性が高く標的を絞った治療を可能にし、生存率の向上と副作用の軽減につながる可能性を持つ。
研究チームにはデューク・シンガポール国立大学(NUS)医学部、NUSがん研究所 (NCIS) およびNUSヨン・ルー・リン医学部の医師と科学者が参加した。チームは2022年1月から2024年12月までの3年間、地理空間技術とゲノム技術を用いて、121人の患者から採取した胃がん検体226個を分析した。
本研究論文の筆頭著者であり、デューク・NUSの研究担当上級副学部長であるパトリック・タン (Patrick Tan) 教授は、「空間技術と遺伝子工学ツールの統合は、古い道路地図をハイテクGPSにアップグレードして、がんを探すようなものです。現在、がん細胞が腫瘍内のどこに存在し、どのように行動し、何が転移や定着の原因となっているのかを正確に特定できます」と語る。
研究チームは、空間トランスクリプトミクスと呼ばれる技術を用いて、腫瘍サンプルの2000個の微小領域からデータを収集し、単一細胞RNAシーケンシングによって15万個の単一細胞を解析した。これら2つの手法を統合することで、胃がん組織の非常に詳細なマップを作成することができた。チームはこれらの手法を組み合わせて腫瘍生態系の高解像度画像を作成し、がん細胞が免疫細胞や血管などの近くの非がん細胞との複雑な相互作用を理解することができた。
同じ腫瘍内に2つのがん細胞のサブグループを見つけたことは、最も重要な発見の一つである。腫瘍の中心部の細胞にはあまり酸素が供給されず、転移する可能性は低いことが分かった。一方、腫瘍の端に存在する細胞は侵襲性が高く、体の他の部位に転移する可能性が高い様子を示した。
これらの違いを理解することは重要である。研究チームは、腫瘍の縁に近いところにある細胞が、特異な非癌性細胞に囲まれていることを発見した。この非癌性細胞は増殖と体の免疫反応に関与することが知られているTGF-β(形質転換成長因子β)と呼ばれるシグナル伝達分子の影響を受けている。将来の治療では、TGF-βシグナル伝達を標的とすることで、腫瘍の防御力を弱め、転移を阻止できるかもしれない。
研究チームはまた、胃がんの複数の進化経路を特定した。それぞれの経路は、病気の進行や治療への反応に独自の影響を与えている。これらの発見は、医師が特定の患者に最適な治療戦略を決定するのに役立つであろう。個別化癌治療への一歩である。
研究チームは現在、胃がん治療のために、さらに多くの治療標的を特定し、前臨床モデルでの試験を行っている。彼らの目標は、それぞれの患者の腫瘍のタイプに合わせた、よりスマートで効果的な治療法を開発することである。






